任天堂Labo纸板玩具推VR套装&结合无现金趋势的智能存钱罐 | 创意新品

▼
之前九方通逊公众号的一篇《你的产品要做FDA申报吗?》文章中有提到:
2)医疗器械范畴,如电动牙刷,按摩器,按摩椅,近视眼镜,太阳眼镜,体温计,血压仪,冲牙器,牙齿矫正器等牙医产品,FDA申报需要:
1 FDA厂家备案号码(FDA factory registration#)
2 产品注册号码( device listing#)
3 初始进口商注册号码(initial US based importer registration#)
4 部分医疗仪器还需要做510K产品售前备案(PremarketNotification 510(k)),如红外线电子体温计,输液泵等,FDA网站上也可以查询是否需要510(k)
www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfpcd/classification.cfm
关于医疗器械进入美国做FDA申报所需的4类资料中,通常第1、第2和第4项都是由厂家自行申请注册完成的,但第3项“初始进口商注册号码”则是由美国的进口商(即买家)注册完成的。对大多数电商货物来说,提供本地进口商都是问题,更别说用进口商完成FDA注册号码了。
很多涉及医疗器械产品的清关问题就出在这,卖家仅有第1、2和第4项却没法提供第3项---初始进口商的FDA注册信息。一旦遇到严格执法的官员,扣货检测折腾几个月后还只能退运甚至销毁。如下例:
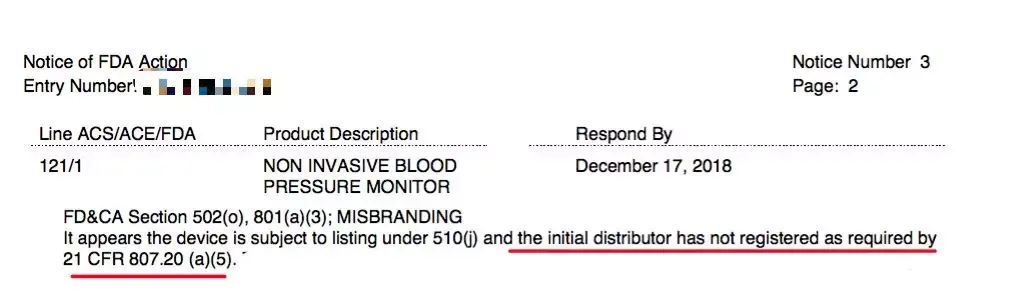
21 CFR 807.20 (a)(5) Acts as an initial importer asdefined in 807.3(g), except that initial importers may fulfill their listingobligation for any device for which they did not initiate or develop thespecifications for the device or repackage or relabel the device by submittingthe name and address of the manufacturer. Initial importers shall also beprepared to submit, when requested by FDA, the proprietary name, if any, andthe common or usual name of each device for which they are the initialimporter;
21 CFR 807.3 (g) Initialimporter means any importer who furthers the marketing of a devicefrom a foreign manufacturer to the person who makes the final delivery or saleof the device to the ultimate consumer or user, but does not repackage, orotherwise change the container, wrapper, or labeling of the device or devicepackage.

为降低风险,按照FDA要求正规申报,那就需要一个美国本土公司作为收货人(即consignee,≠Importer of Record),并注册initial USbased importer registration#。九方通逊针对本身已经满足第1、2和第4项条件的医疗器械类产品推出一项服务:为客户 提供第3项FDA初始进口商注册号码 来协助完成清关,具体服务详情可咨询我司客户经理。
(当然,我们可以提供服务以满足FDA在资料和资质上的要求,但如果产品本身经不起FDA抽查,尤其是检测,那就还是不要来冒这个险了)
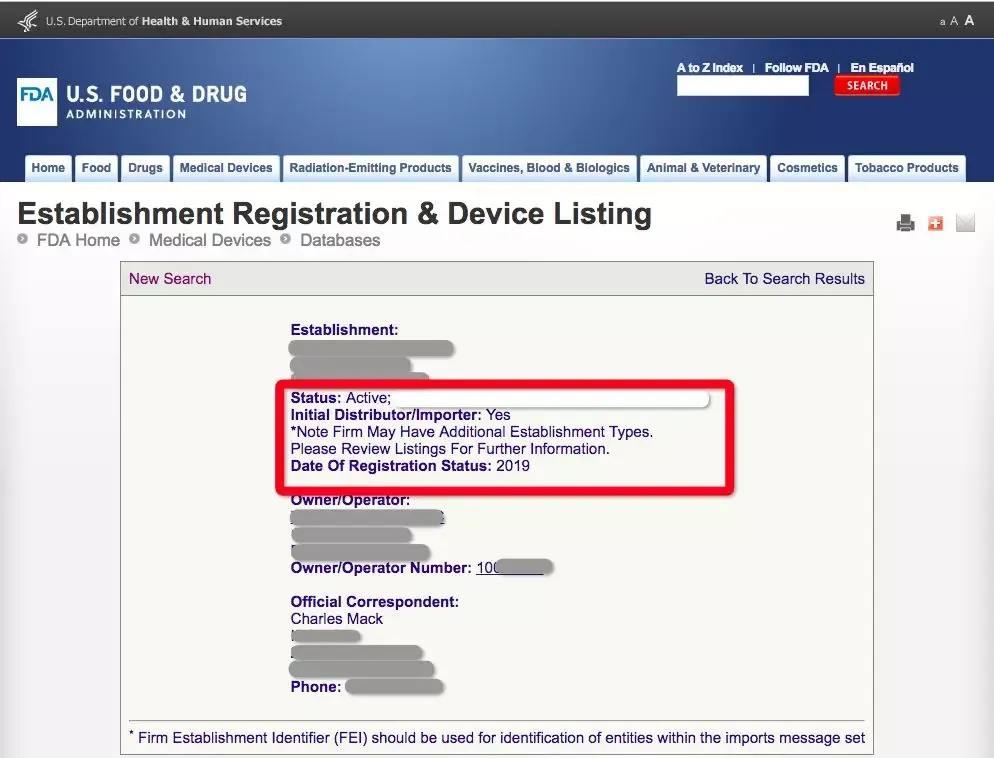
(初始进口商注册号码有效记录)

我们建了一个亚马逊卖家交流群,里面不乏很多大卖家。
现在扫码回复“ 加群 ”,拉你进群。
热门文章
*30分钟更新一次