近期口罩出口真可谓是“大浪淘沙”,一波未平一波又起…
25日晚,商务部、海关总署、国家市场监督管理总局发布联合公告(2020年第12号),4月26日起加强非医用口罩出口质量监管,公告全文如下:

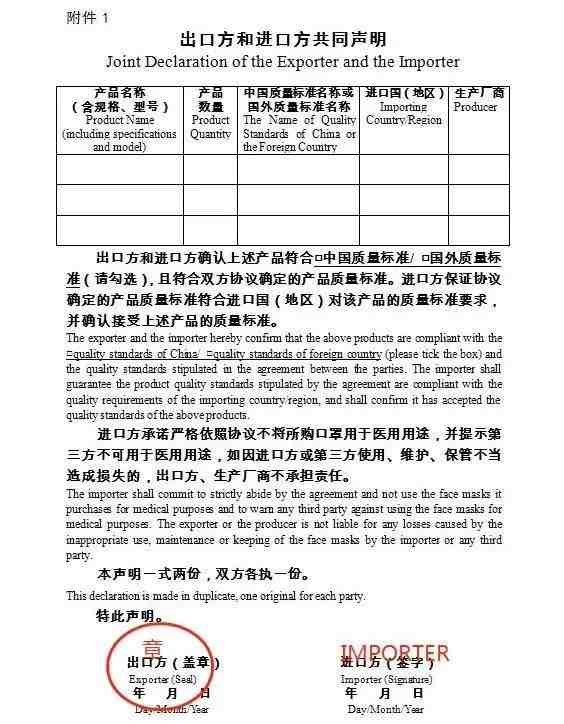
在全球疫情持续蔓延的特殊时期,为更有效支持国际社会共同应对全球公共卫生危机,现就进一步加强防疫物资质量监管、规范出口秩序有关措施公告如下:一、加强非医用口罩出口质量监管。自4月26日起,出口的非医用口罩应当符合中国质量标准或国外质量标准。商务部确认取得国外标准认证或注册的非医用口罩生产企业清单(中国医药保健品进出口商会网站www.cccmhpie.org.cn动态更新);市场监管总局提供国内市场查处的非医用口罩质量不合格产品和企业清单(市场监管总局网站www.samr.gov.cn动态更新);非医用口罩出口企业报关时须提交电子或书面的出口方和进口方共同声明(参考附件1),确认产品符合中国质量标准或国外质量标准,进口方接受所购产品质量标准且不用于医用用途,海关凭商务部提供的企业清单验放,对不在市场监管总局提供的企业清单内的,海关接受申报,予以验放。
对4月26日之前已签订的采购合同,出口报关时须提交电子或书面的出口方和进口方共同声明(参考附件1)。二、进一步规范医疗物资出口秩序。自4月26日起,产品取得国外标准认证或注册的新型冠状病毒检测试剂、医用口罩、医用防护服、呼吸机、红外体温计的出口企业,报关时须提交书面声明(参考附件2),承诺产品符合进口国(地区)质量标准和安全要求,海关凭商务部提供的取得国外标准认证或注册的生产企业清单(中国医药保健品进出口商会网站www.cccmhpie.org.cn动态更新)验放。以上防疫物资出口质量监管措施将视疫情发展情况动态调整。
对于新政策的推出,可以分两部分进行解读:
25日晚24点前已经进监管区尚未放行的货物。需要买卖双方签署《出口方和进口方共同声明》,而后可被获准放行而不受名单影响。但是如果在不合格名单范围中,则可能还是不允许出口。4月26日0点后申报出口的货物,必须同时满足以下三个条件:1、在商务部确认取得国外标准认证或注册的非医用口罩生产企业清单范围内或符合国内质量标准;2、不在市场监管总局提供国内市场查处的非医用口罩质量不合格产品和企业清单内;对于非医用口罩应当符合中国质量标准或国外质量标准的要求,应该分为三种情况:1、国外强制要求执行相关标准的,并且采用生产商准入制度的,则应以公布名单为准。2、国外官方认可中国质量标准予以替代的,比如美国FDA的紧急使用授权法案就明确,符合YY/T0969的用于医护领域的就不用FDA认证,欧盟也是符合GB2626的用于医护的现在不用办CE。3、国外对非医用口罩无相关执行标准的,则必须符合中国质量标准。所以,中国质量标准和境外标准不是“或”的关系。对于符合中国质量标准的判定,可能需要以第三方检测机构的报告为宜,目前还未看到海关可以以企业自检报告作为替代的,当然不排除执行差异问题。
自4月26日0时起,出口包括医用口罩在内的2020年第5号公告的医疗物资范围中的产品,在公告基础上增加了以下两项要求:1、商务部提供的取得国外标准认证或注册的生产企业清单;
这意味着企业既要中国的医疗器械注册,还要符合境外的标准认证或注册,并纳入国外官方准入清单。从公告中提到的《国外标准认证或注册的非医用口罩生产企业清单》来看,非医用口罩也必须取得进口国官方的注册和企业准入,这将进一步提高对非医用口罩的监管要求,而这个要求则符合业内人士在之前的猜测,即对出口产品的监管责任主要在于进口国,只要进口国认可了产品或生产企业,中国海关没必要再做限制性措施。在公告中有一个特殊的措辞 “对4月26日之前已签订的采购合同” ,对于这个合同签署节点确认的问题,海关应该是无法确定的,所以可能会以是否已经申报作为标志进行 “一刀切” 的判断;也很可能海关以申报时间为准。当然,这只是一种猜测,具体还要以执行为准, 这个问题的执行就有待海关进一步明确了。
针对商务部12号公告,大家最关心的主要问题有:
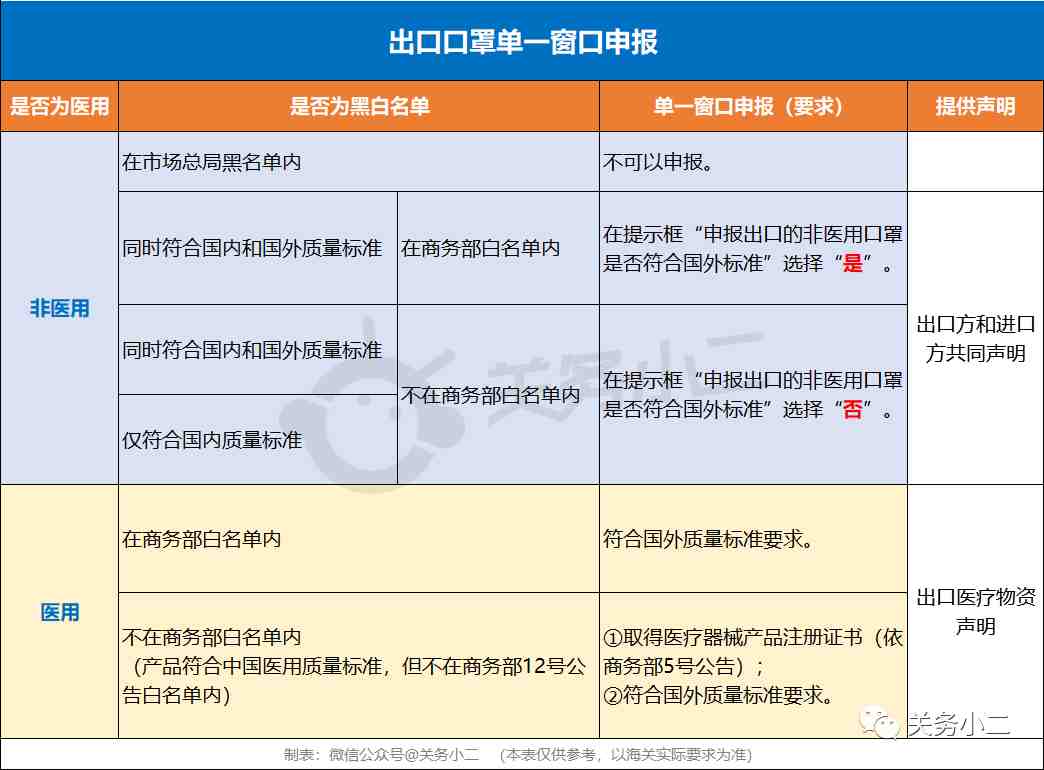
1.非医用口罩仅符合国内质量标准,但不在商务部白名单中,能否正常出口?2.非医用口罩同时符合国内和国外质量标准,但不在商务部白名单中,能否正常出口?3.医用口罩等医用物资符合中国医用质量标准,但不在商务部白名单,能否正常出口?4.商务部5号公告和12号公告是冲突还是关联的关系?为方便大家理解,小编专门做了一张表格图:
一、出口非医用口罩
1.非医用口罩出口实行白黑名单管理,商务部提供白名单,市场监管总局提供黑名单。符合国外质量标准看商务部白名单(需在名单内);国内质量标准看市场监管总局黑名单(需不在名单内)。
换句话说就是非医用口罩只要在黑名单内的就不可以申报。
不在黑名单也不在白名单的,只要产品符合我国质量标准的也可以正常申报,申报时多提供一个双方共同声明就行。
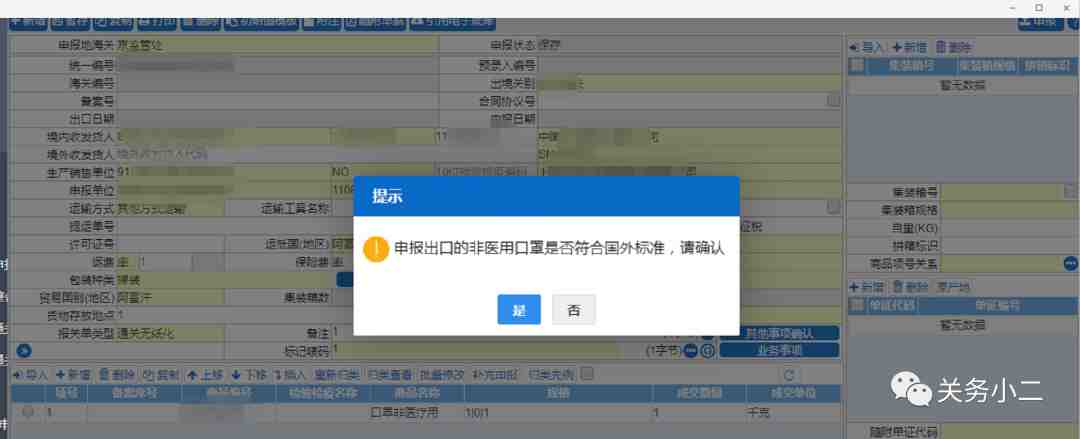
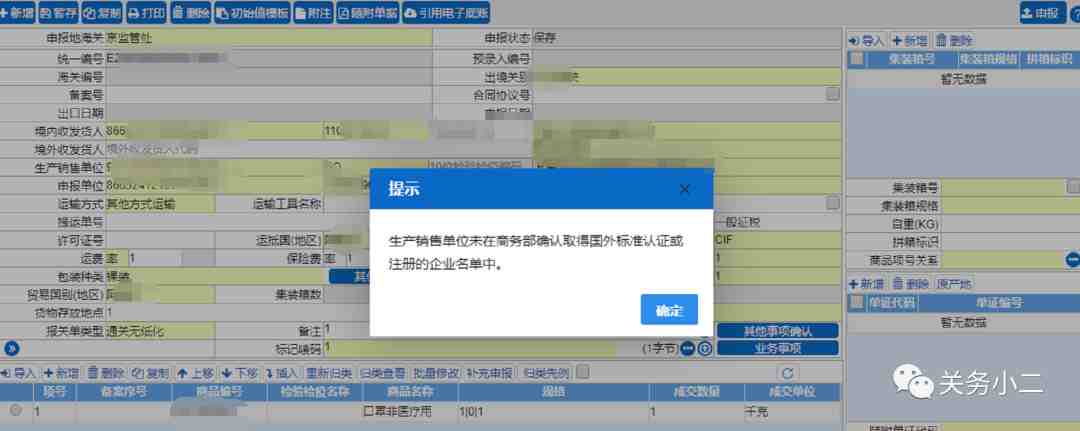
2.目前,单一窗口系统已更新,填报时,在出口报关单的“生产销售单位”栏目填写实际生产口罩企业名称及代码(不填销售企业),并点击是否符合国外标准,此时,单一窗口系统会将申报的生产企业名单与商务部提供的白名单进行核碰,核碰上的,则自动受理申报。
二、出口医疗物资
商务部12号公告,自4月26日起,产品取得商务部白名单的新冠病毒检测试剂、医用口罩、医用防护服、呼吸机、红外体温计的出口企业,海关凭商务部白名单验放(企业提供出口医疗物质声明,可免提交医疗器械产品注册证)。
不在商务部12号公告白名单内但产品符合中国医用质量标准的,按照商务部5号公告执行,企业需取得医疗器械产品注册证书,并提供出口医疗物资声明承诺符合国外质量标准要求。
如果是4月1日(含)以后签订合同且出口产品未取得医疗器械产品注册证书的生产企业,但是符合国外质量标准要求,生产企业可向当地商务局申请加入商务部白名单。申请说明详见本公众号4月26日次头条推文。
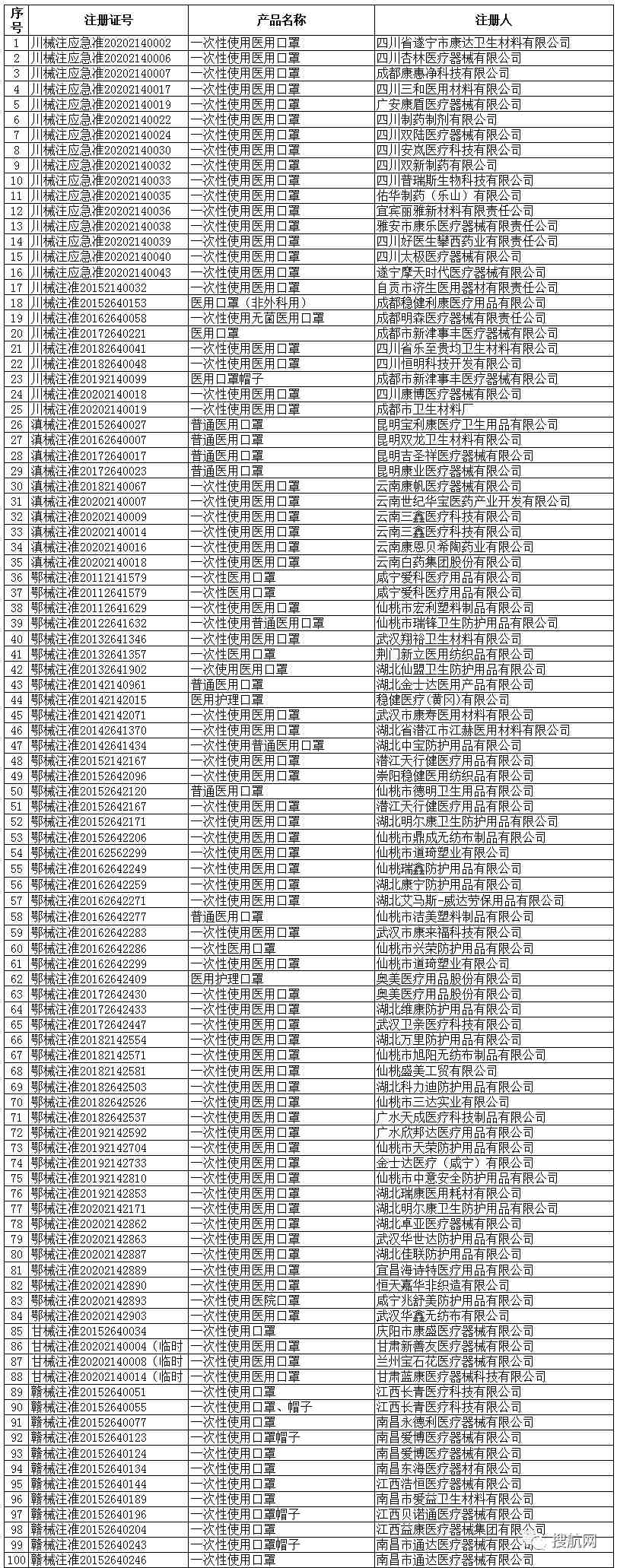
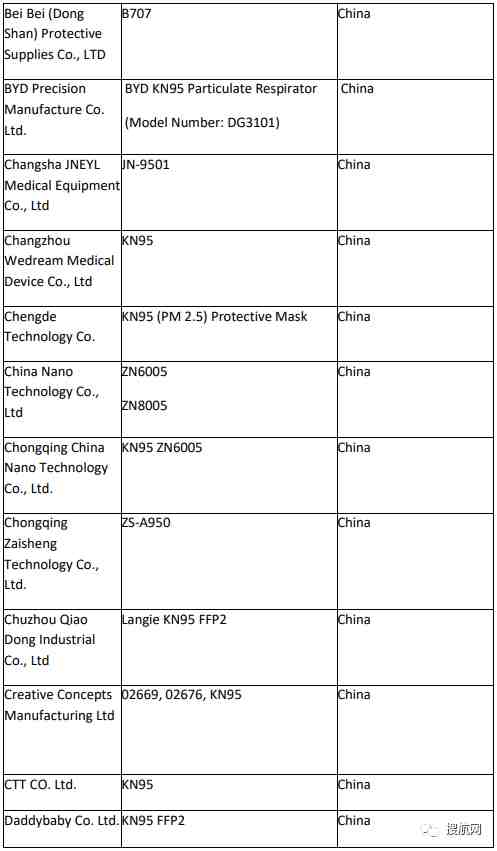
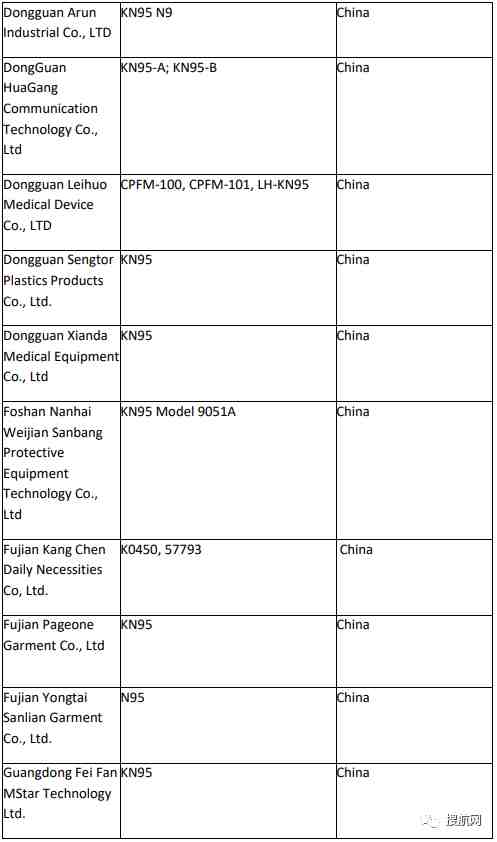
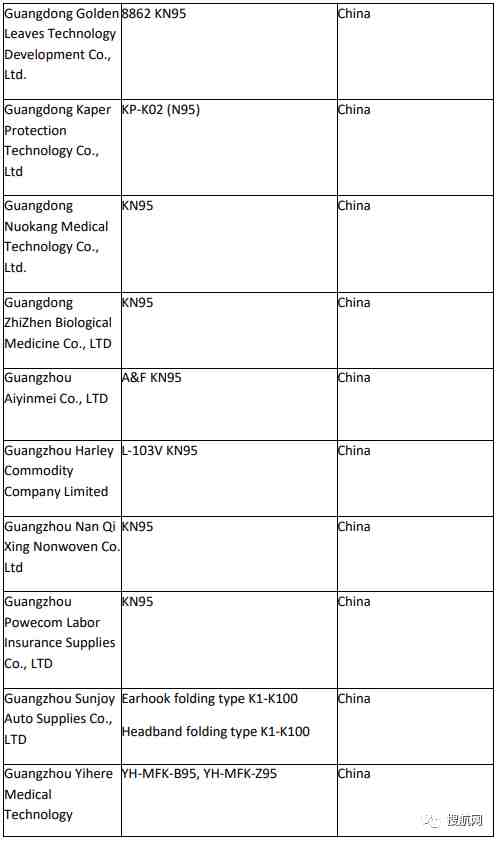
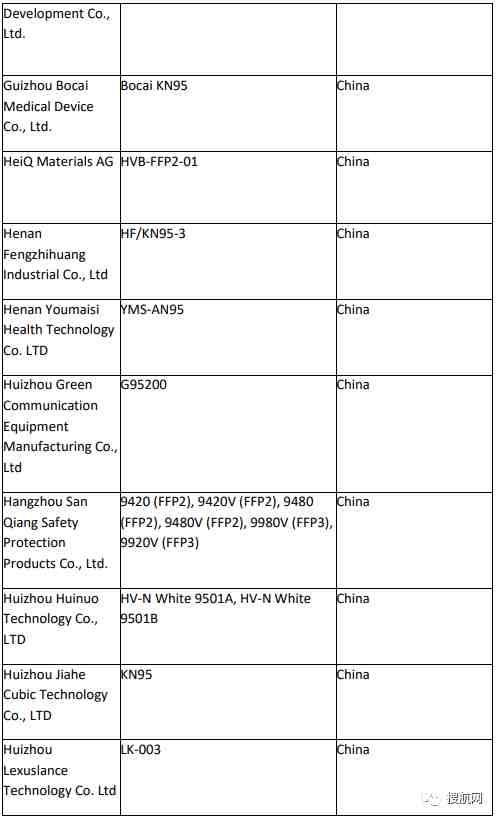
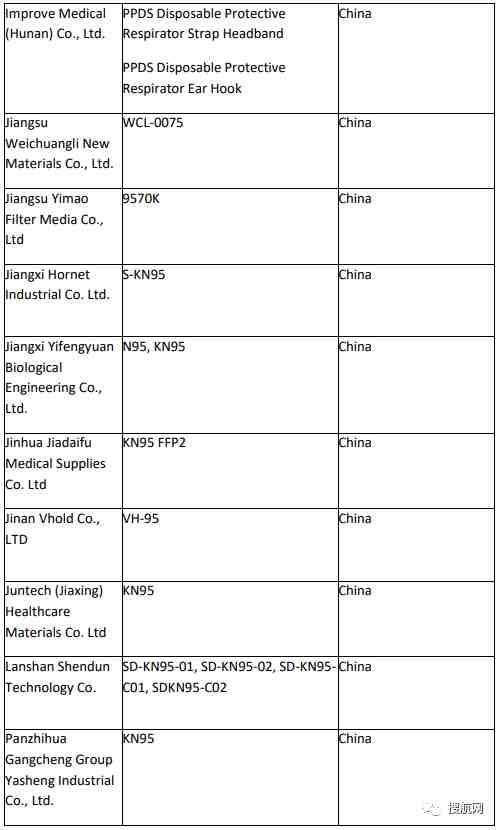
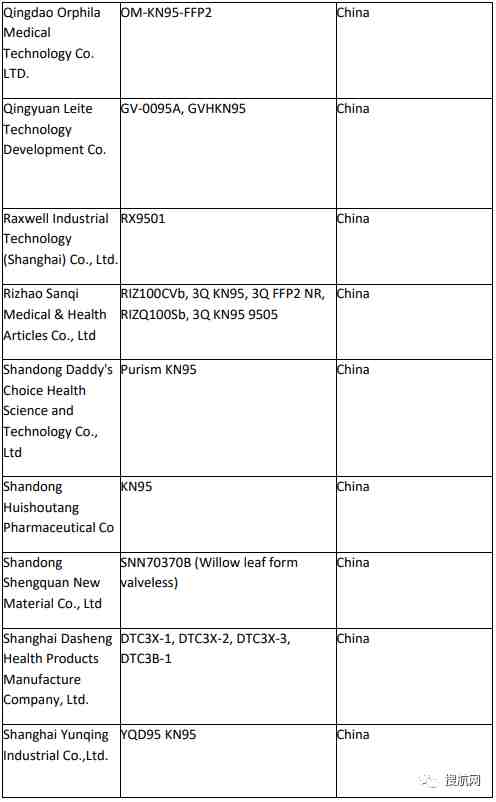
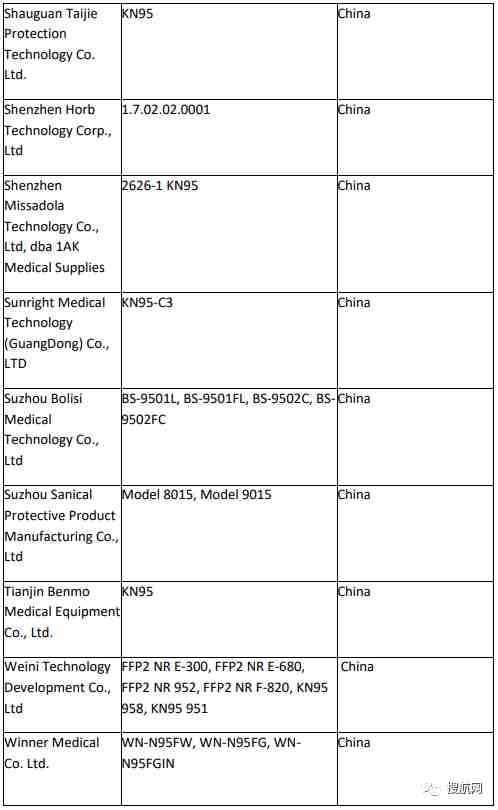
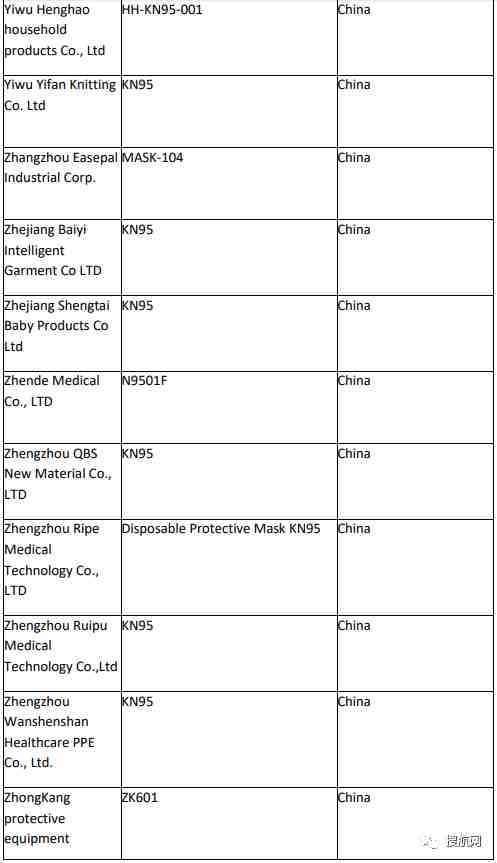
附:非医用口罩生产企业白名单:
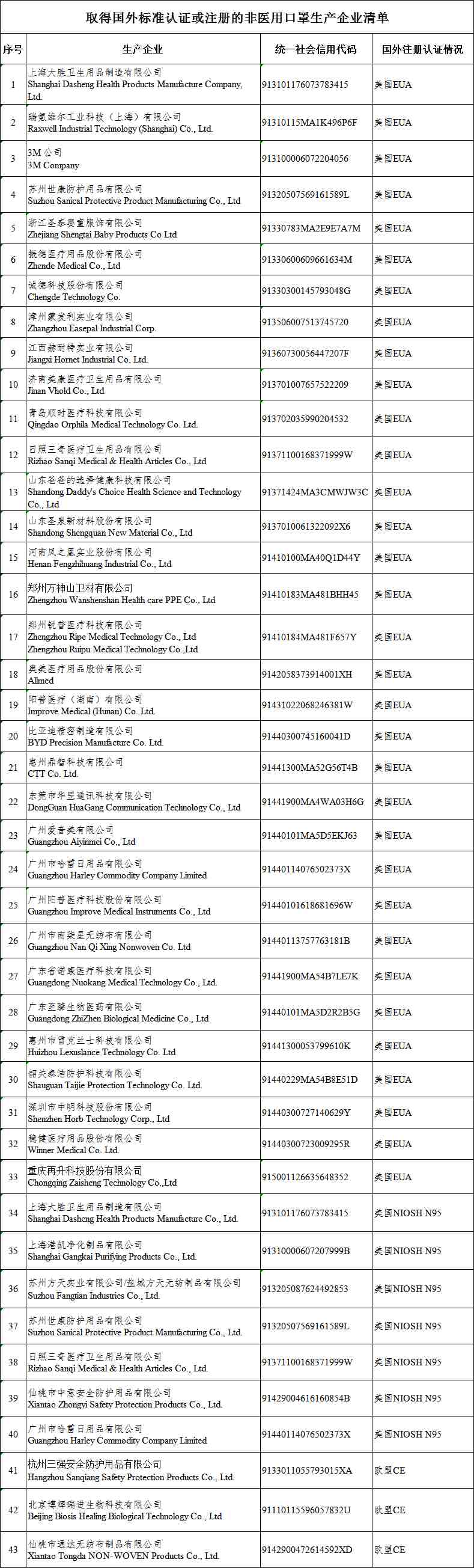
已取得国外标准认证或注册的医疗物资生产的白名单企业:

另外中国商务部在4月1日实施的第5号公告中,已公布首批取得我国医疗器械产品注册证书的“白名单”企业。
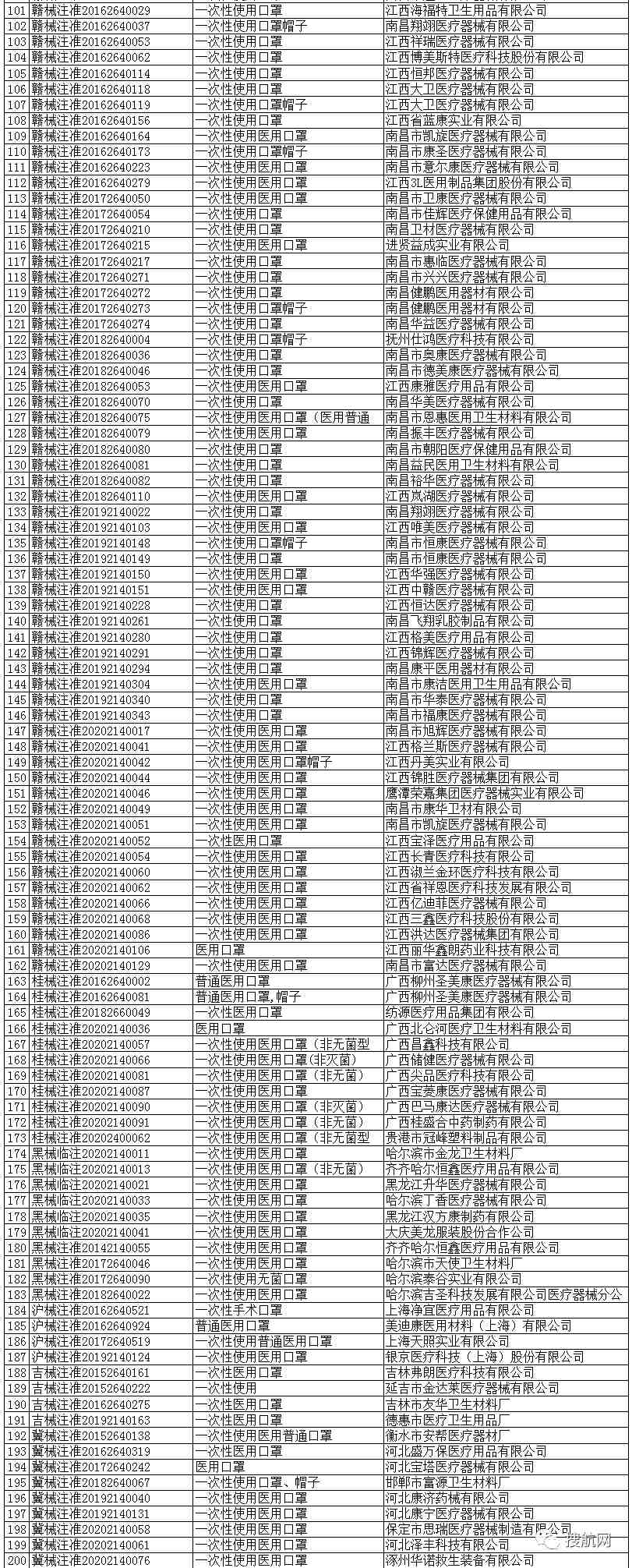
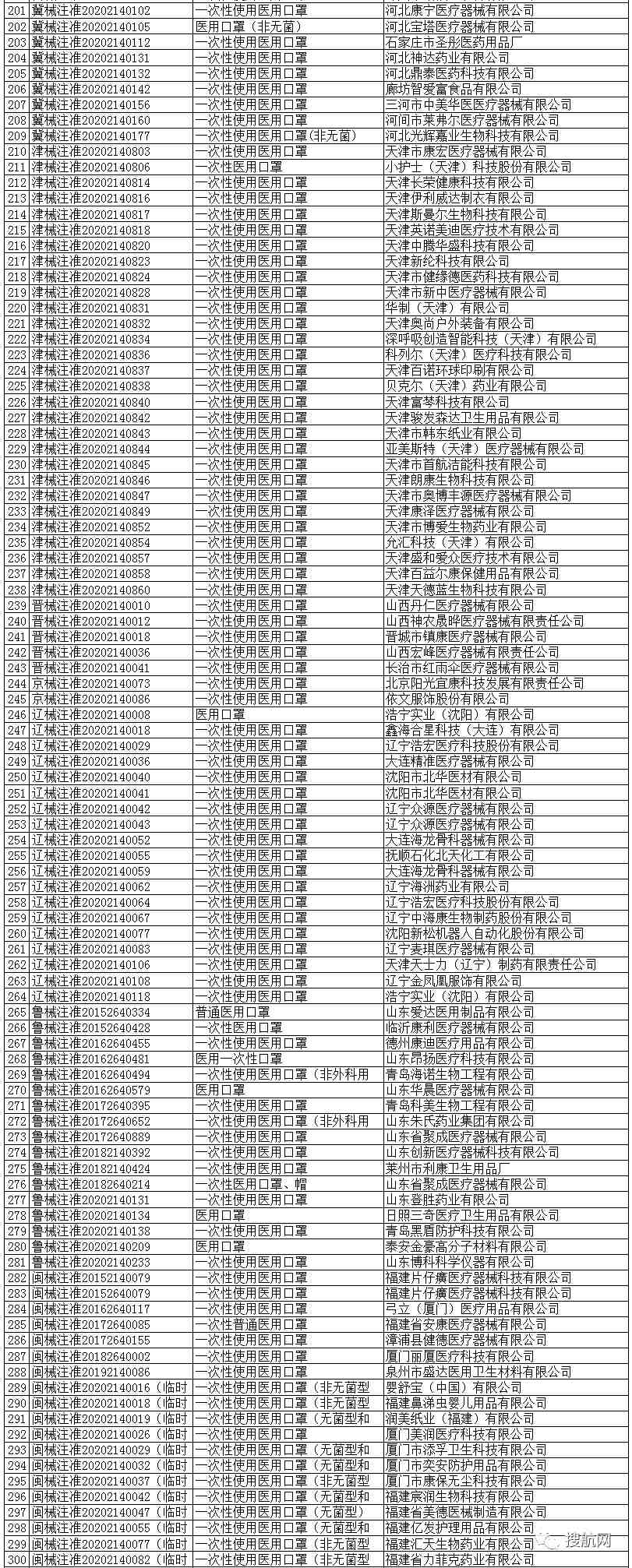
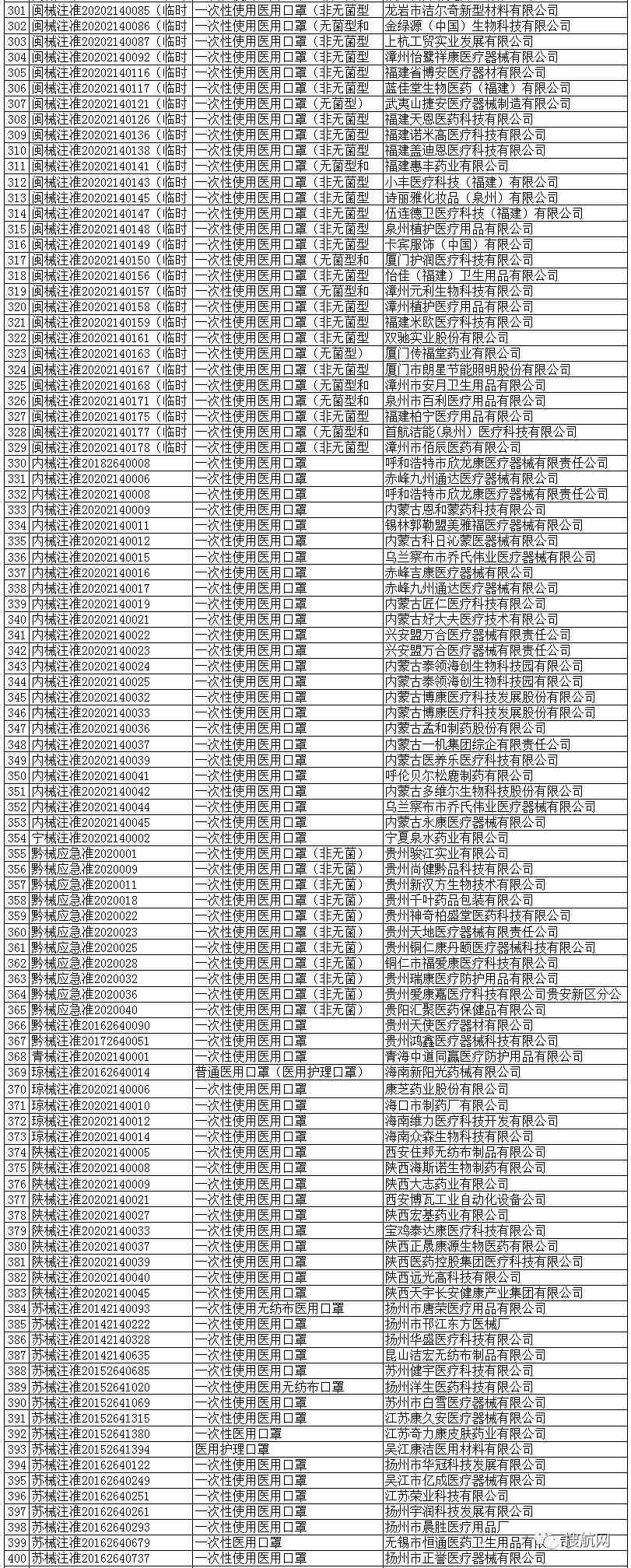
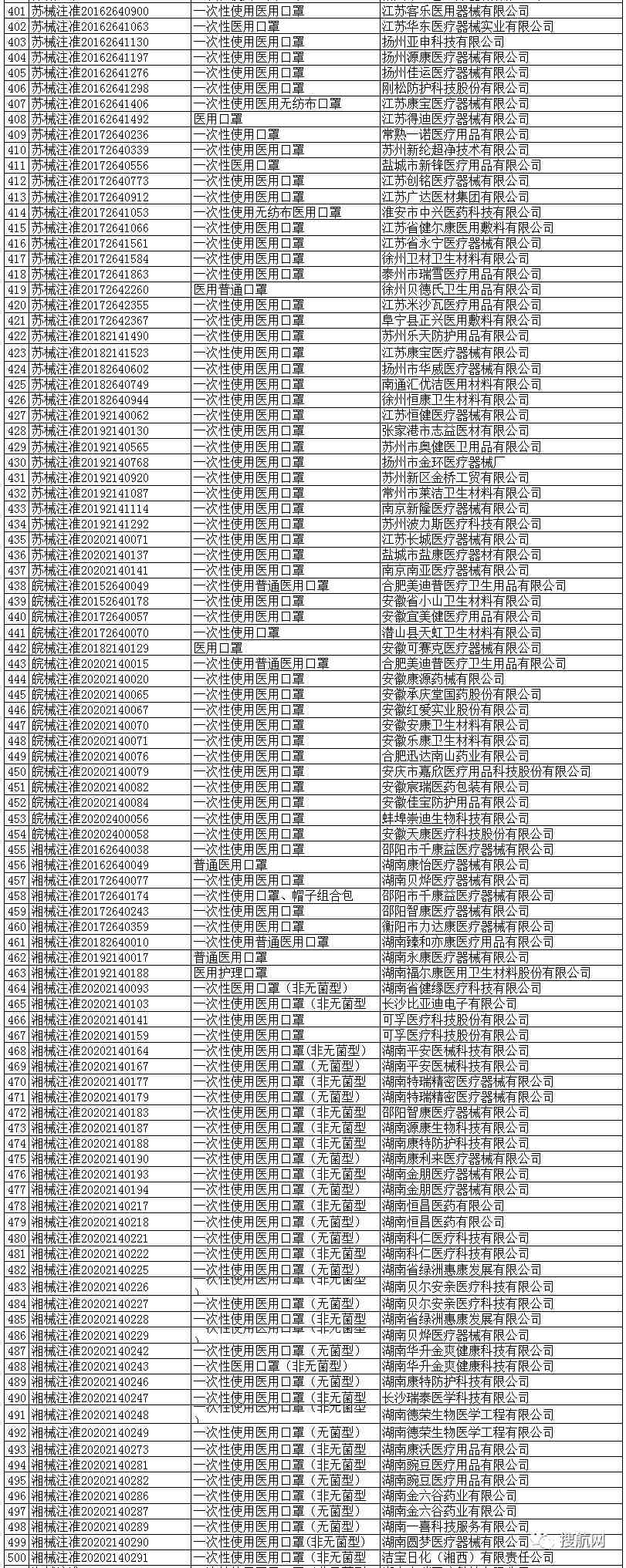
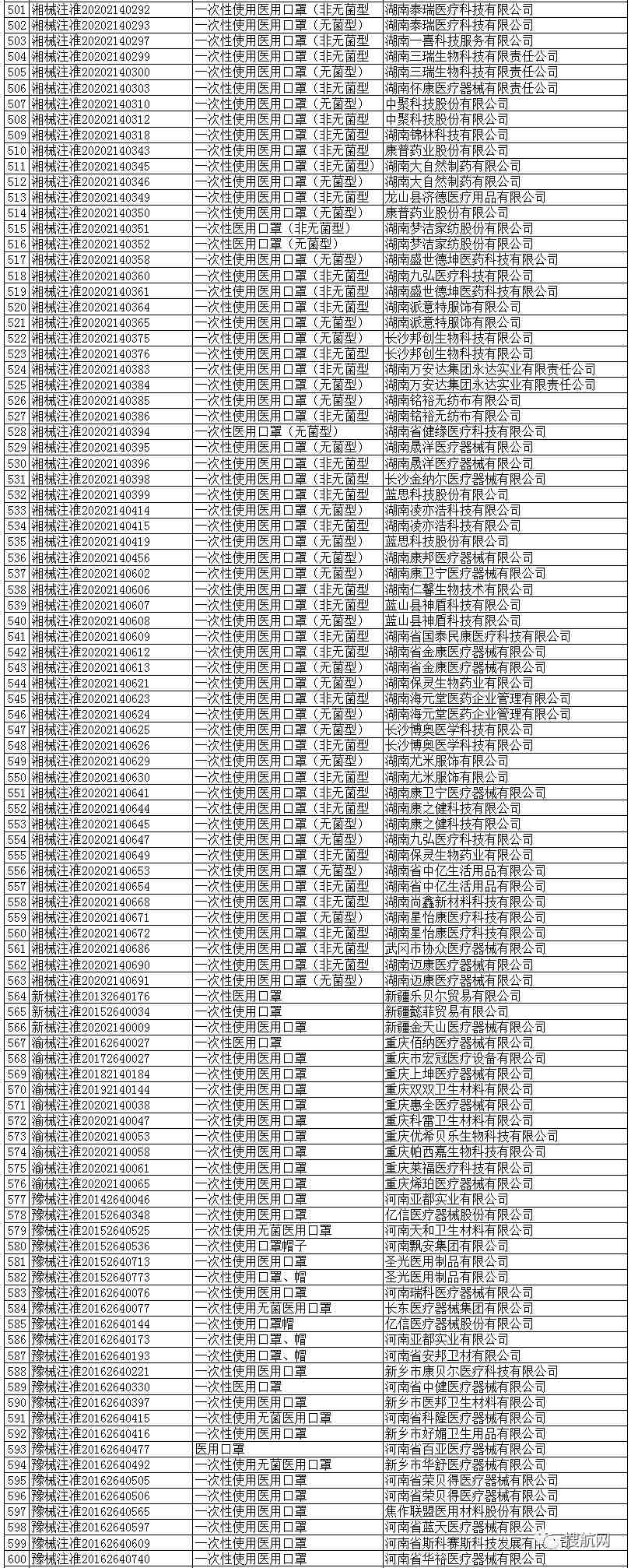
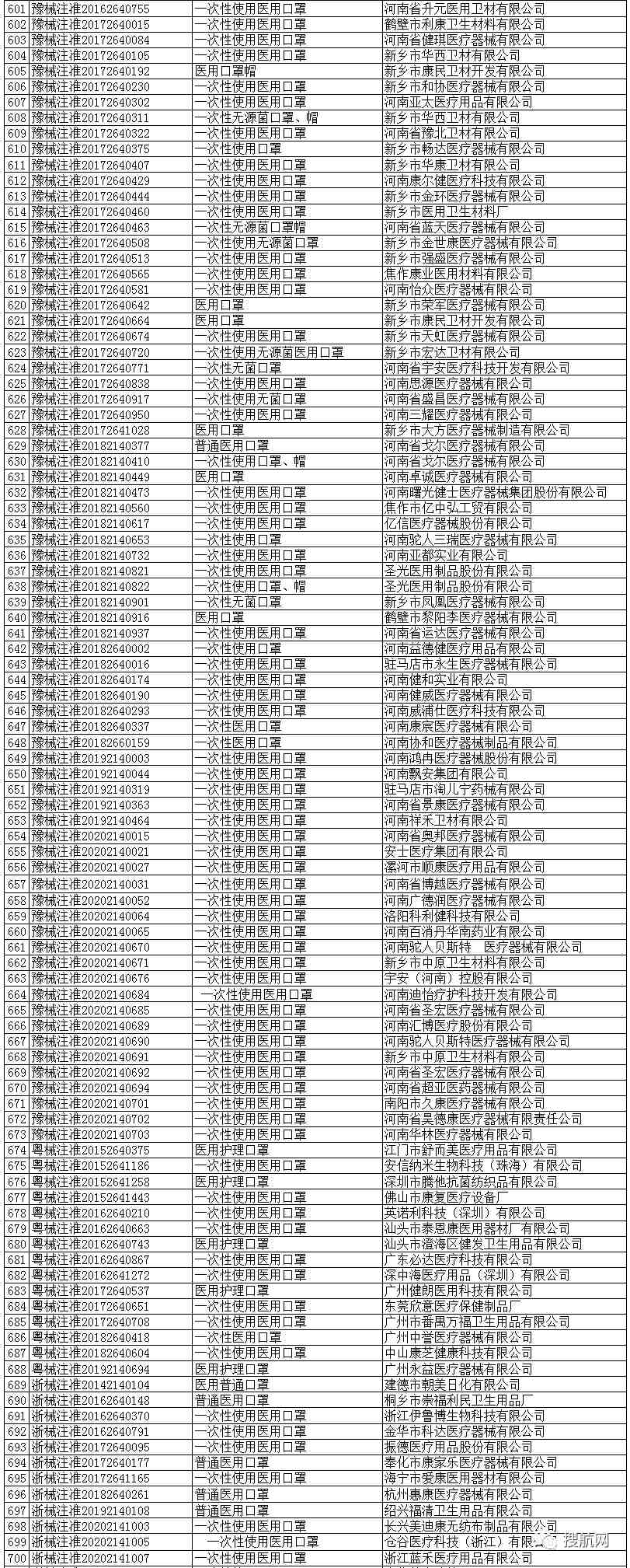
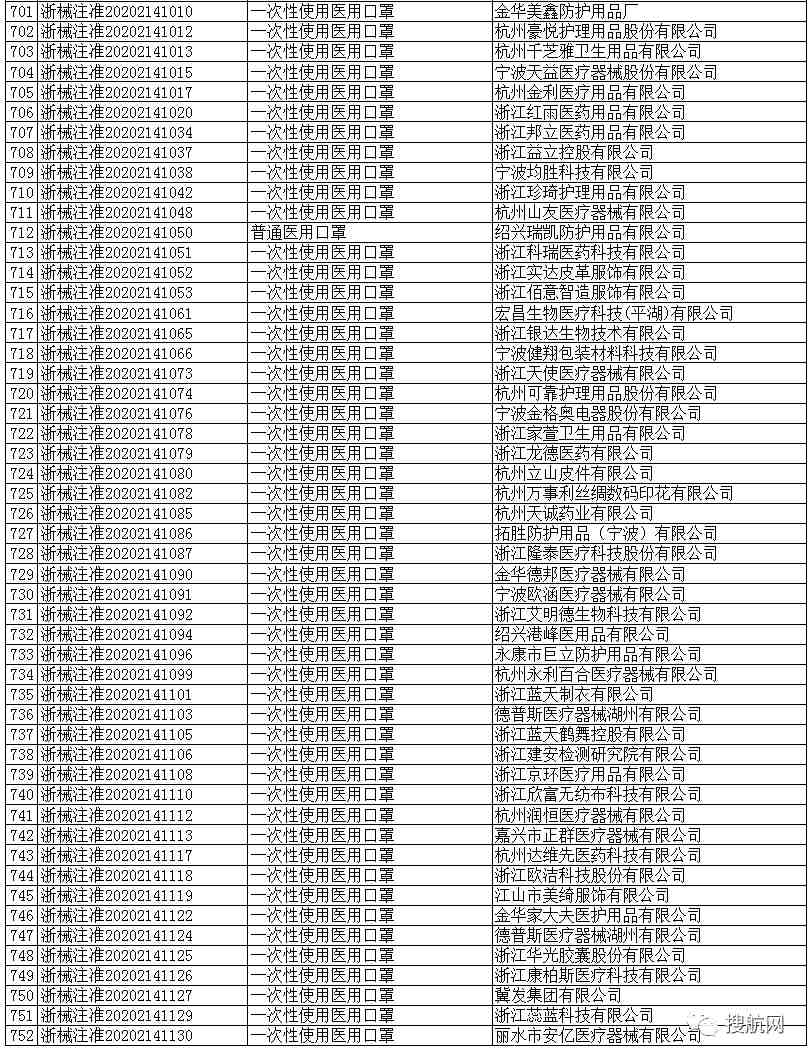
一次性使用医用口罩(共752家)
医用防护口罩(共150家)
省级药监部门医用防护口罩注册信息
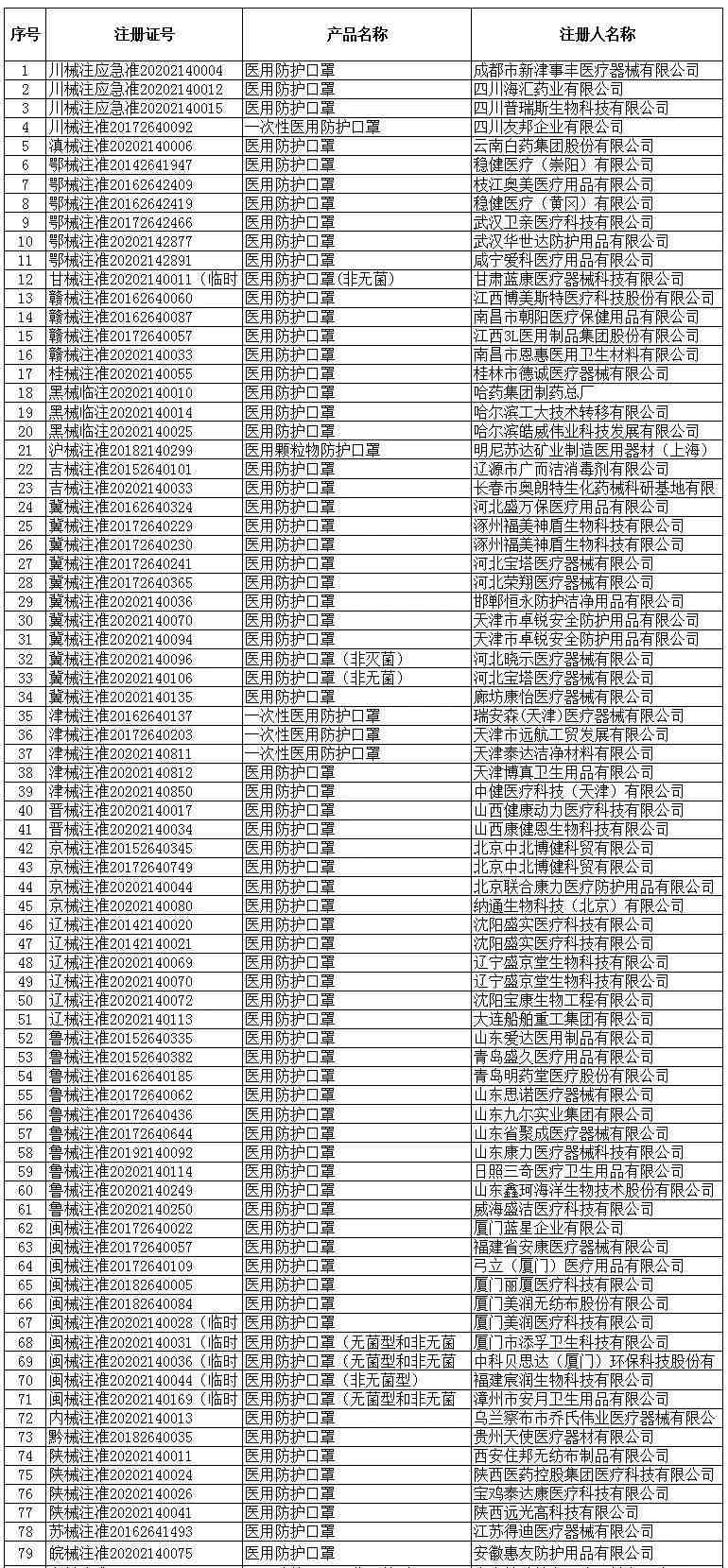
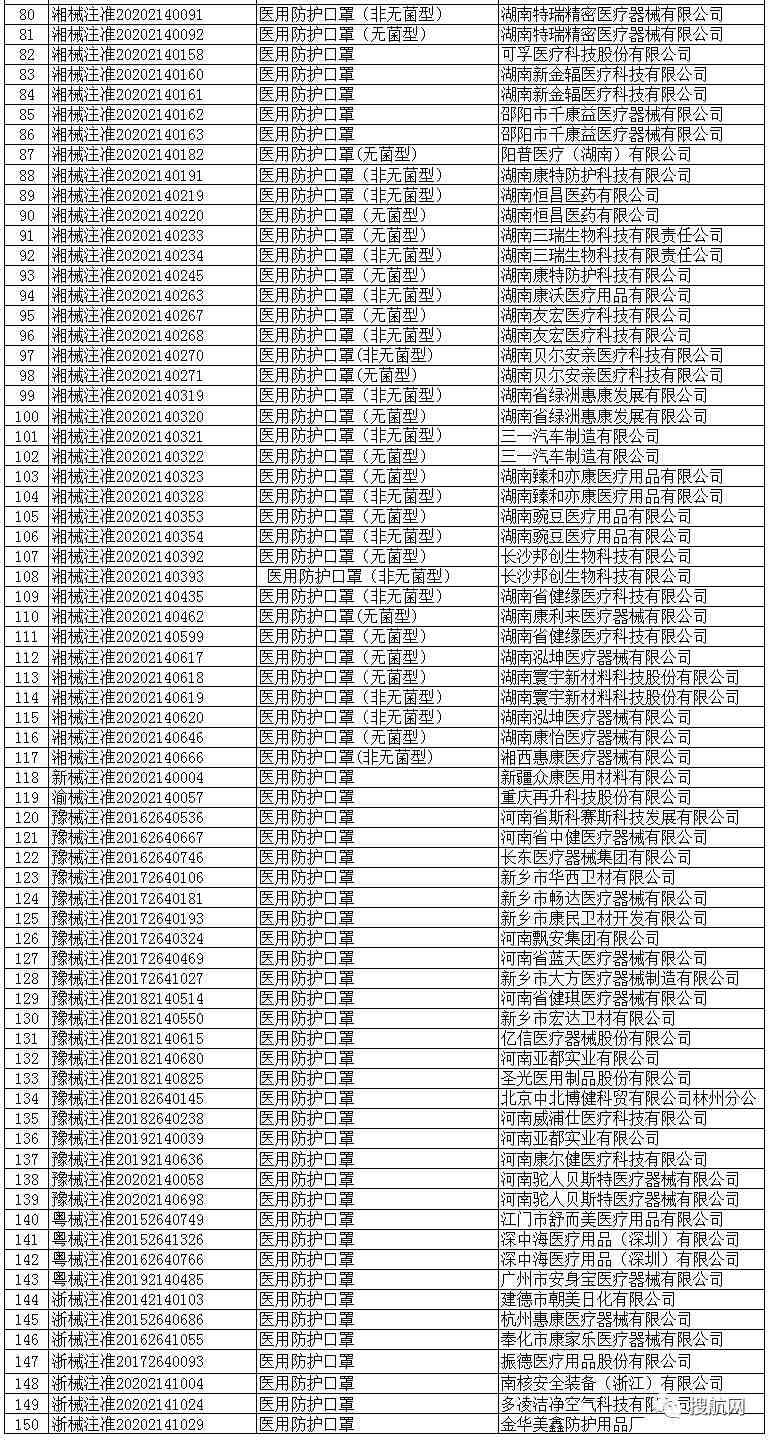
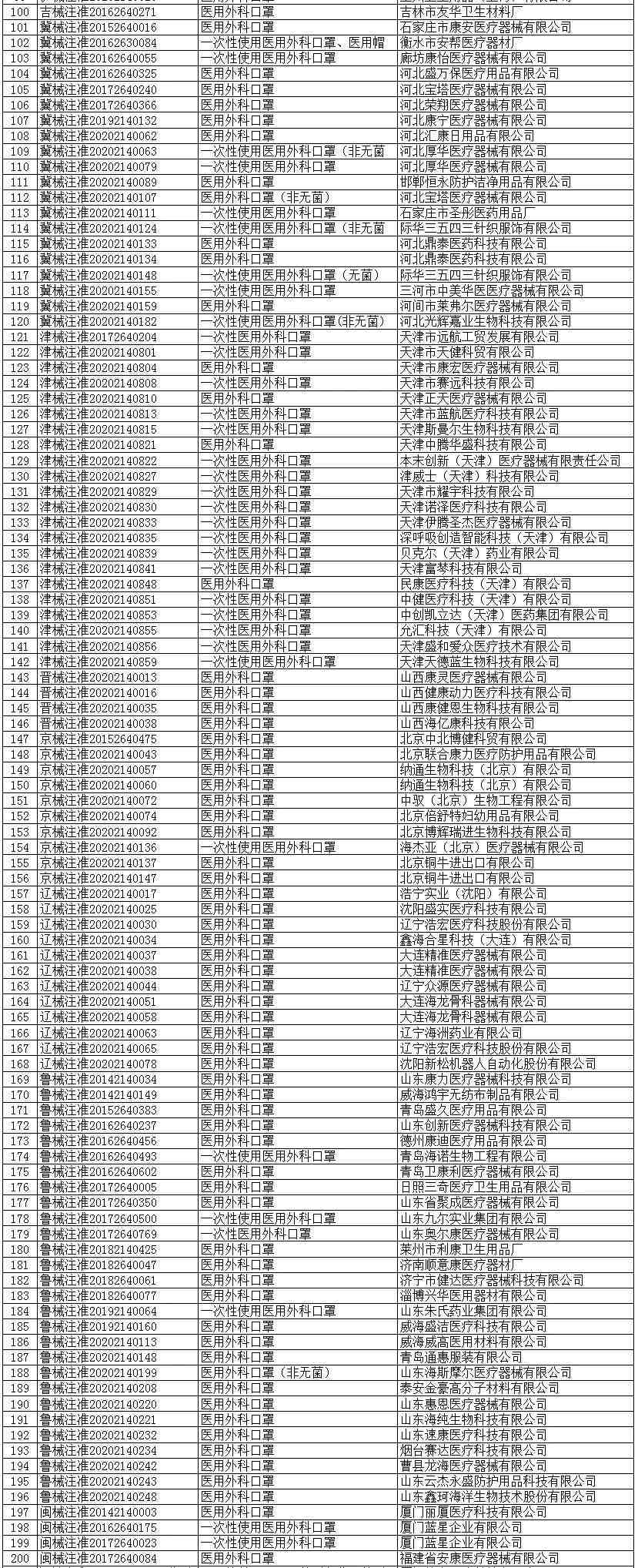
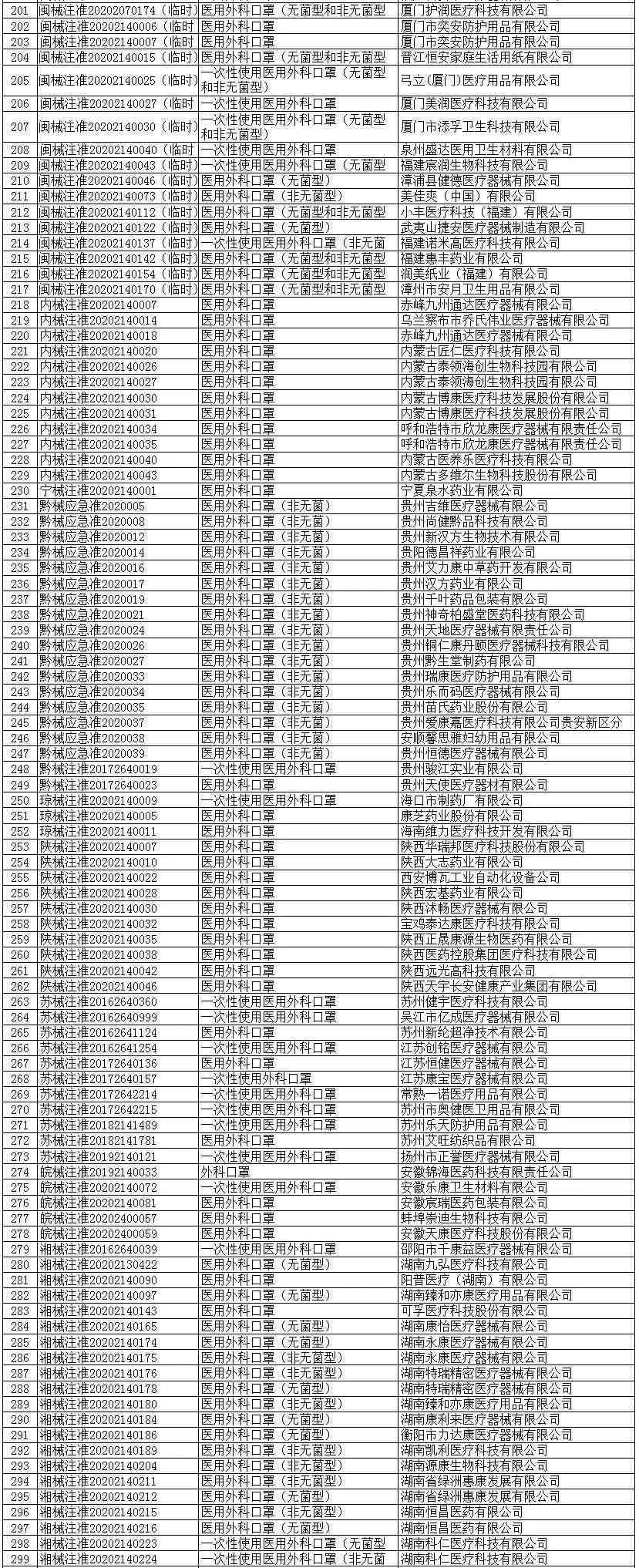
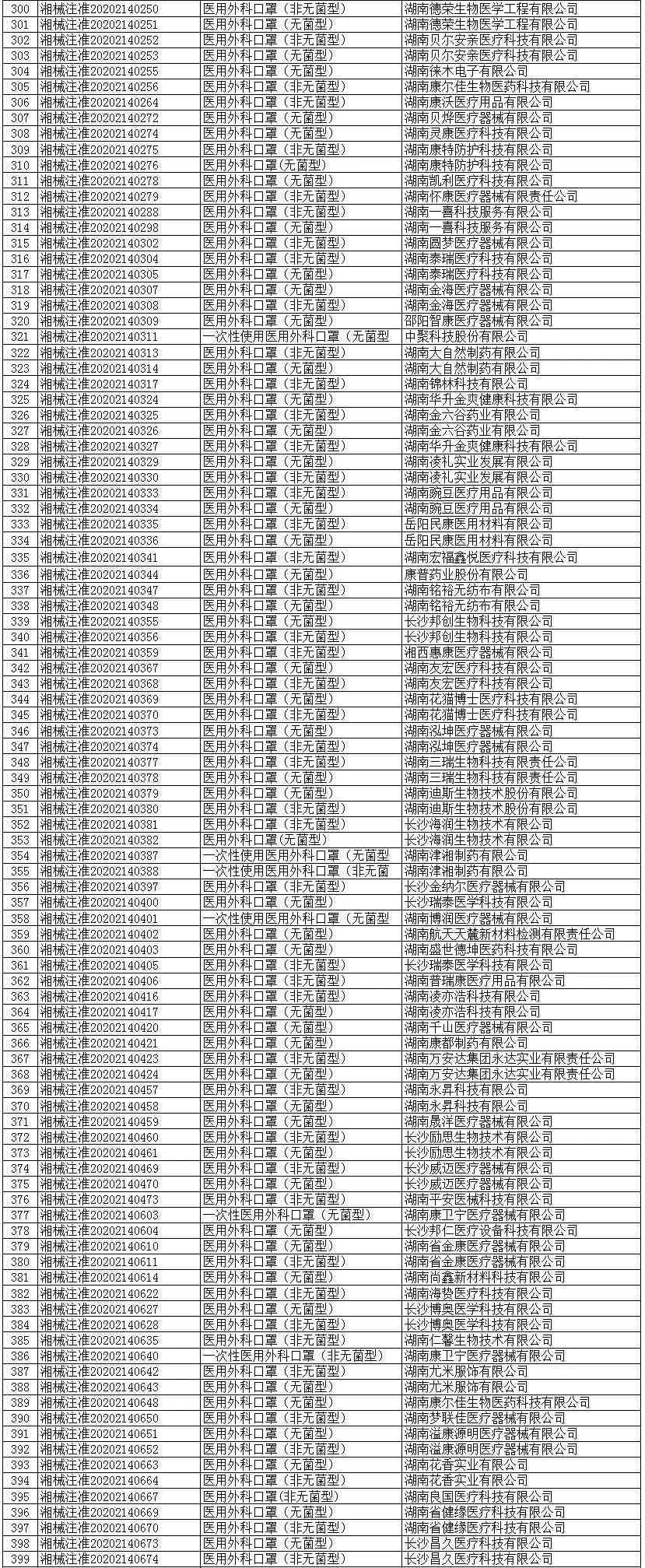
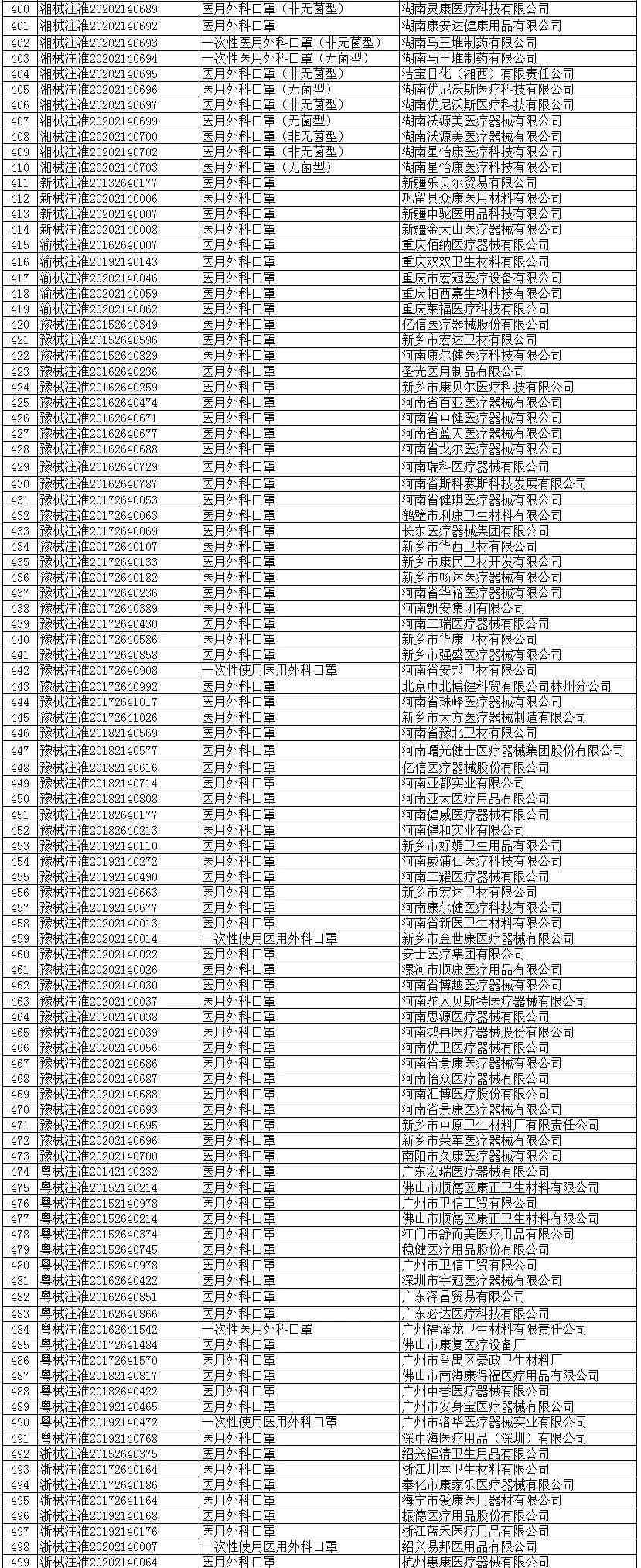
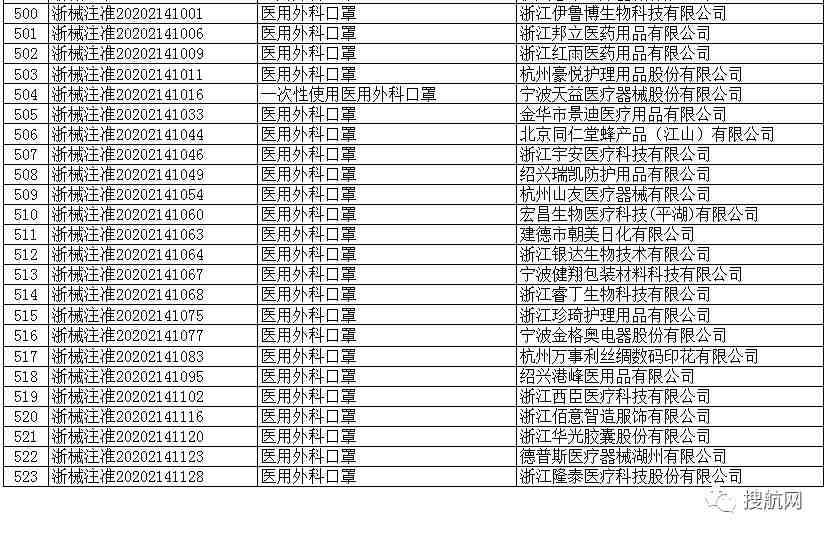
医用外科口罩(共523家)
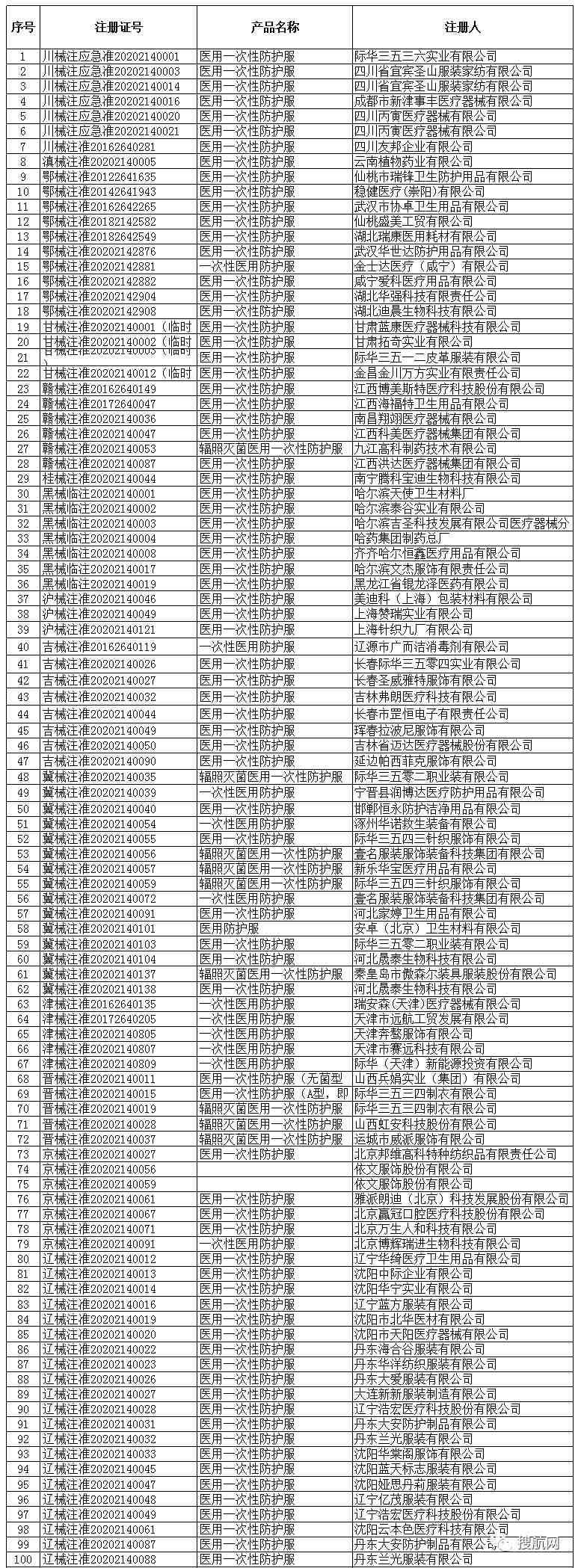
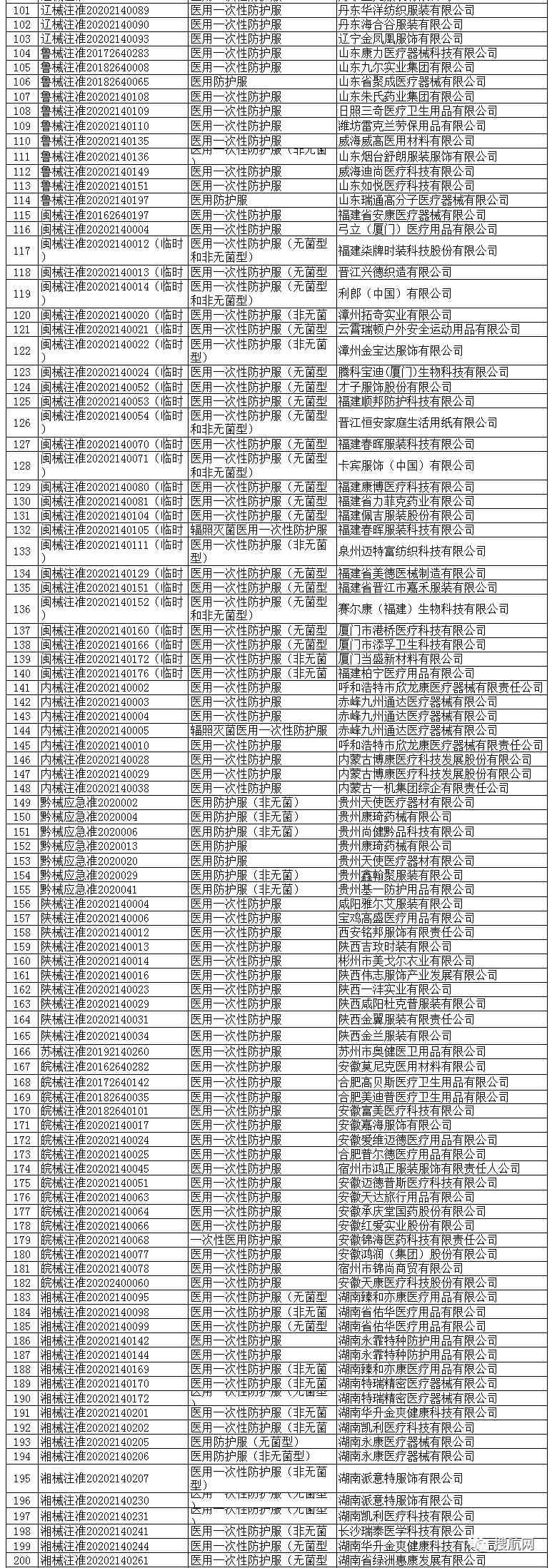
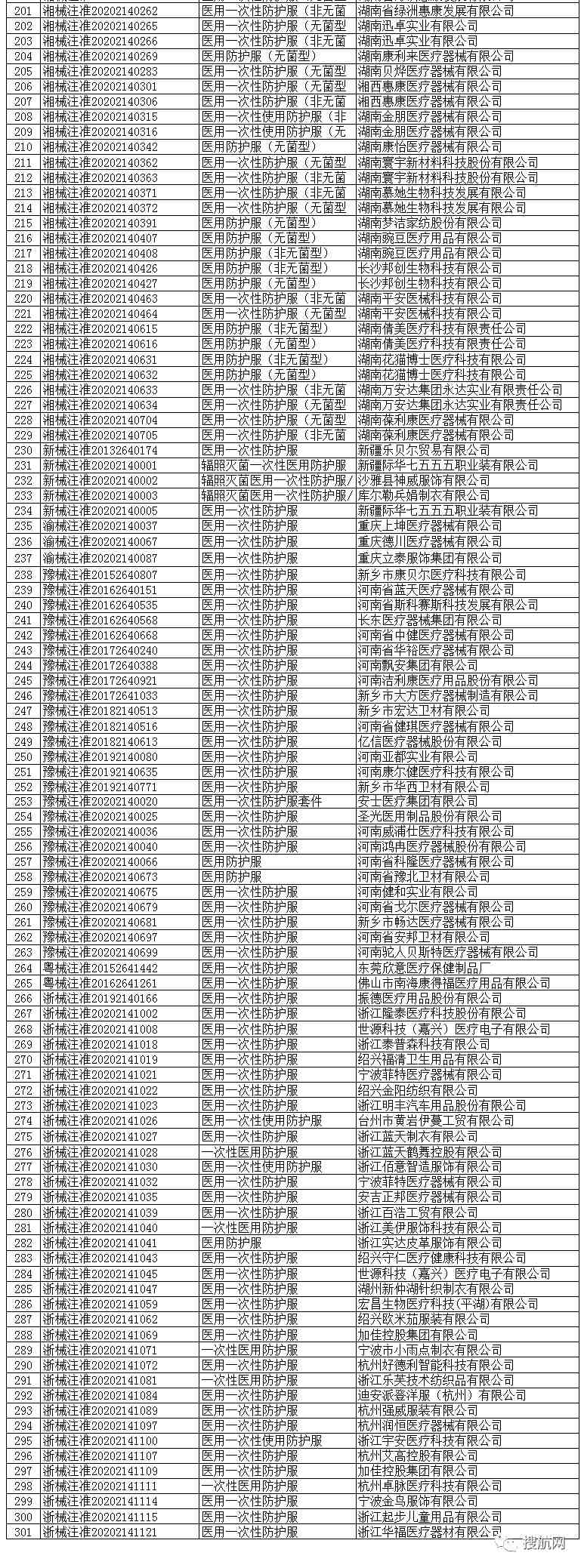
医用防护服(共301家)
新冠病毒检测试剂(共23家)
省级药监部门新型冠状病毒检测试剂注册信息
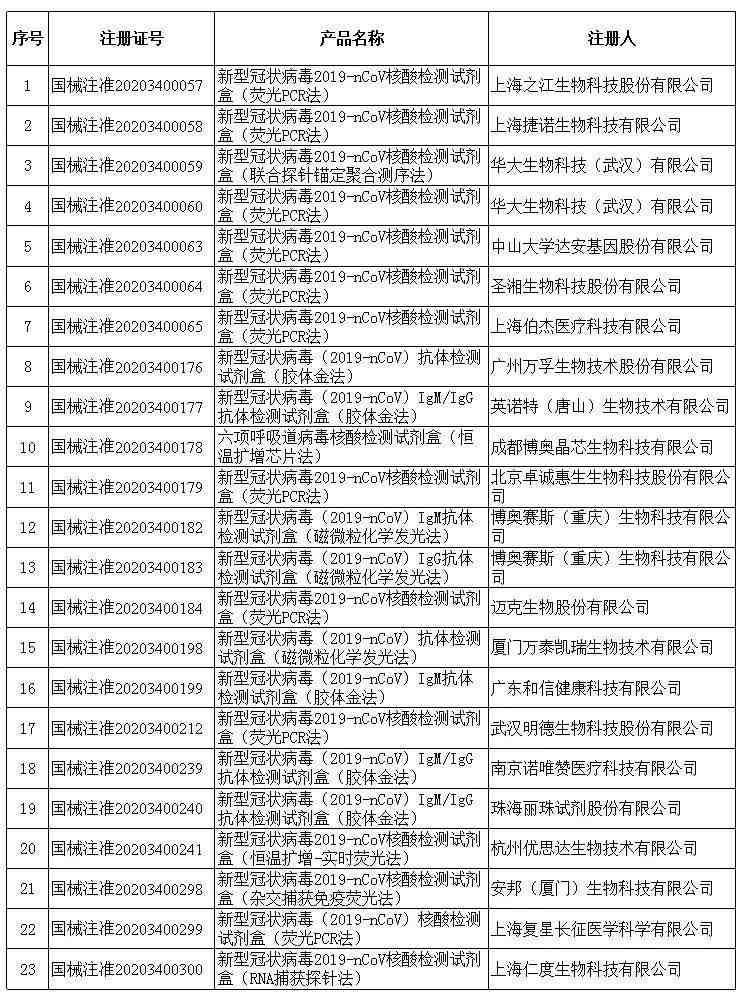
呼吸机(共62家)
国家及省级药监部门国产呼吸机注册信息
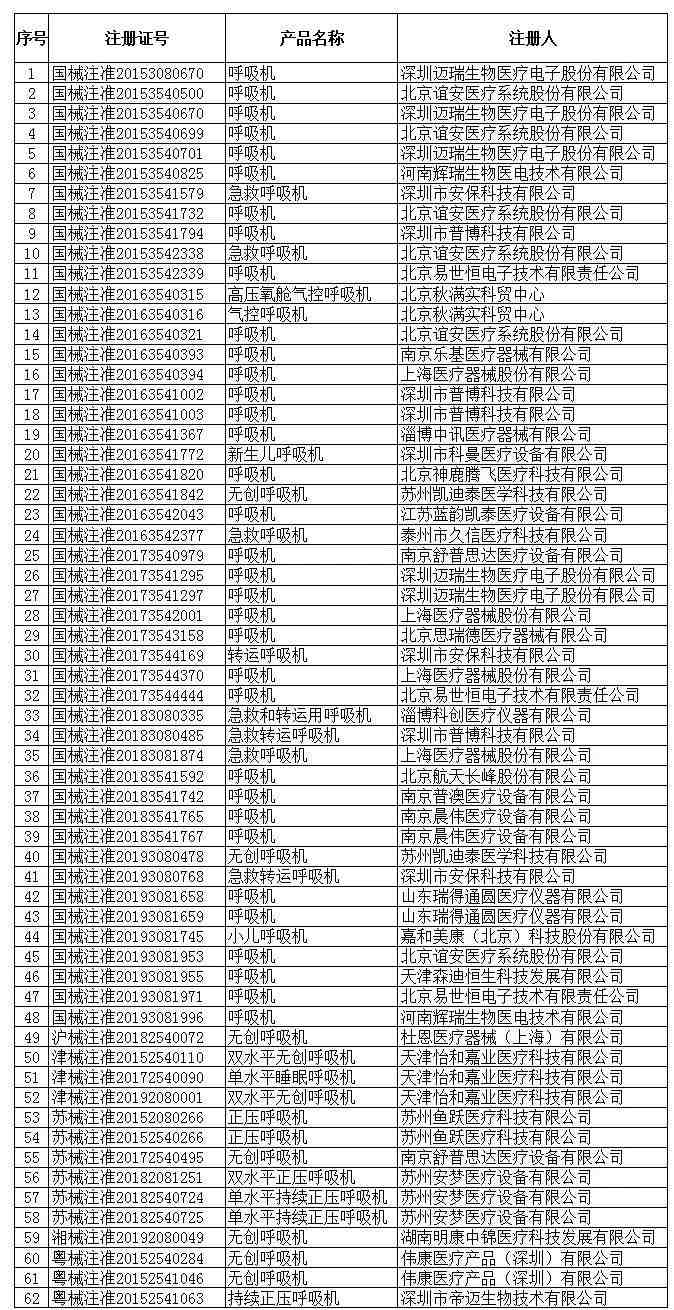
红外体温计(共236家)
省级药监部门红外体温计(含耳温计、额温枪)注册信息
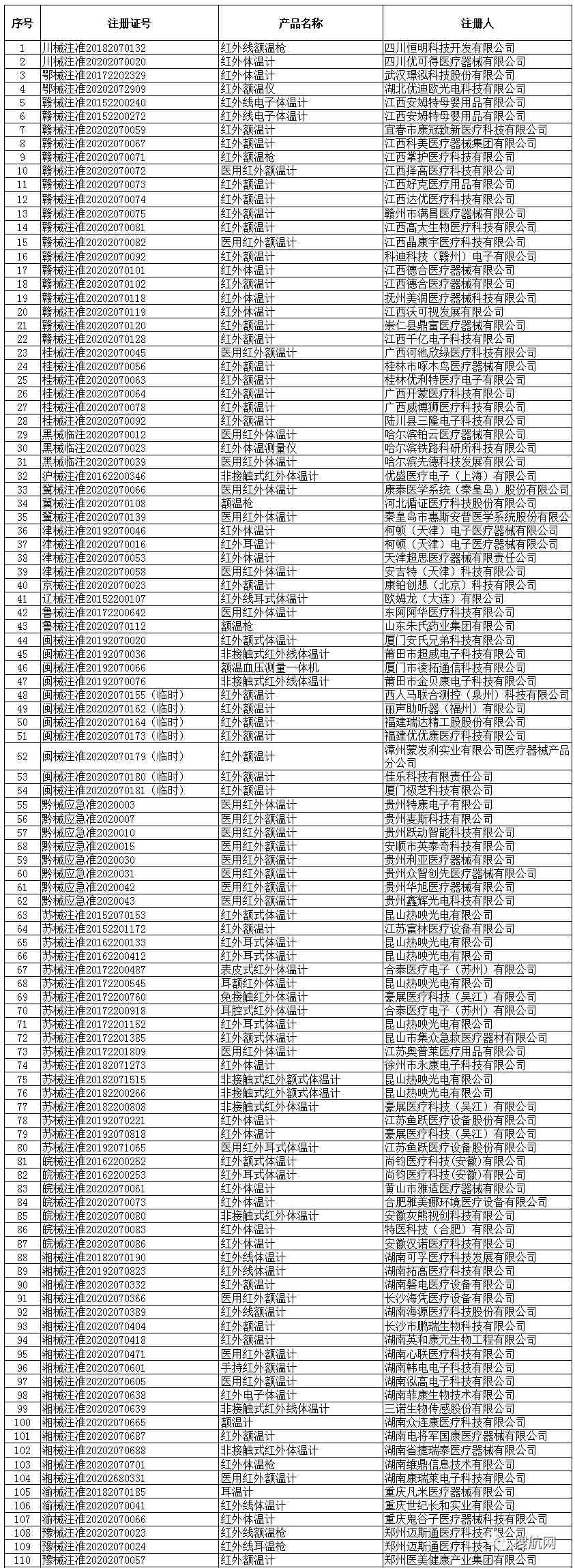
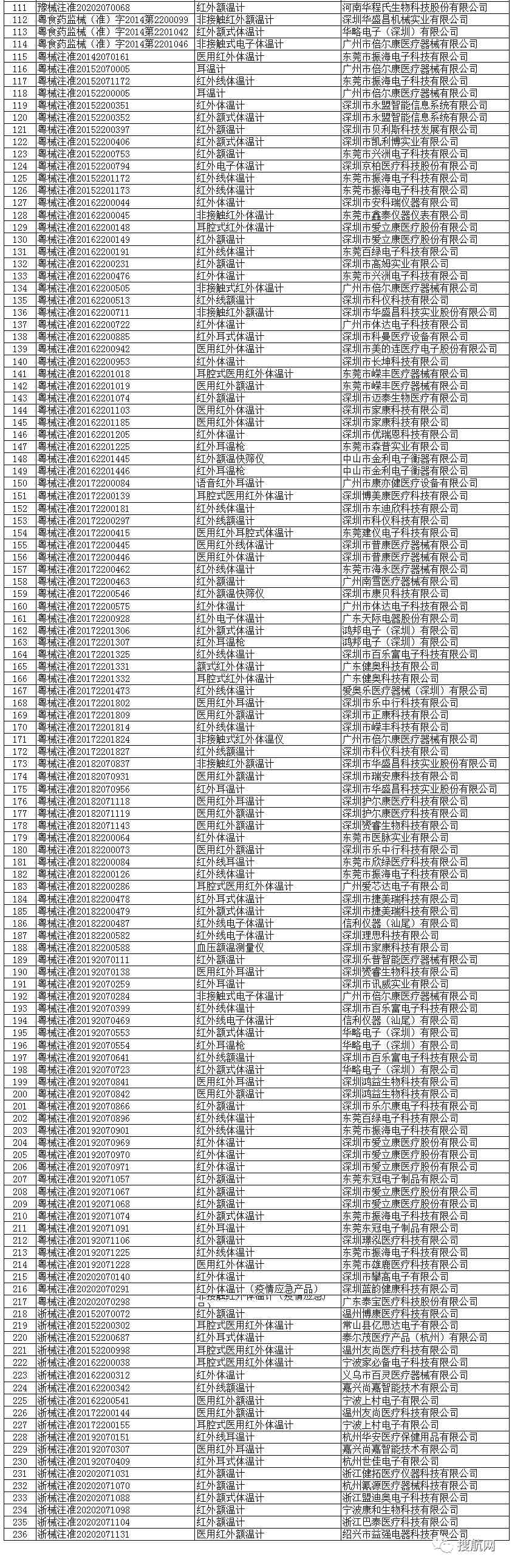
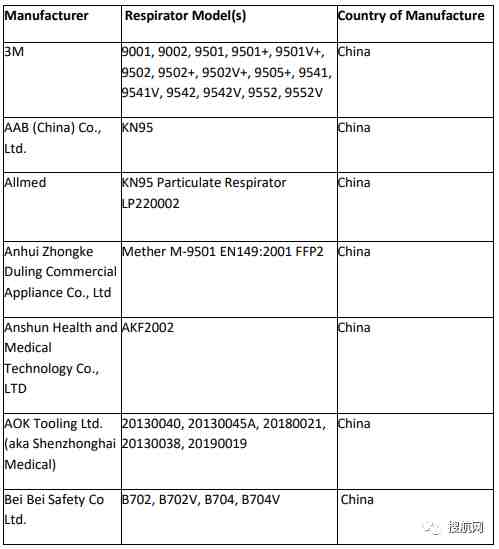
此外,美国食品药品监督管理局(FDA)也更新了最新获得美国授权并认可的中国企业名单:
除了白名单的企业,随着近期中国海关以及海外对口罩等防疫物资的严查,已经有数十家认证企业和生产出口企业被列入了”黑名单“。
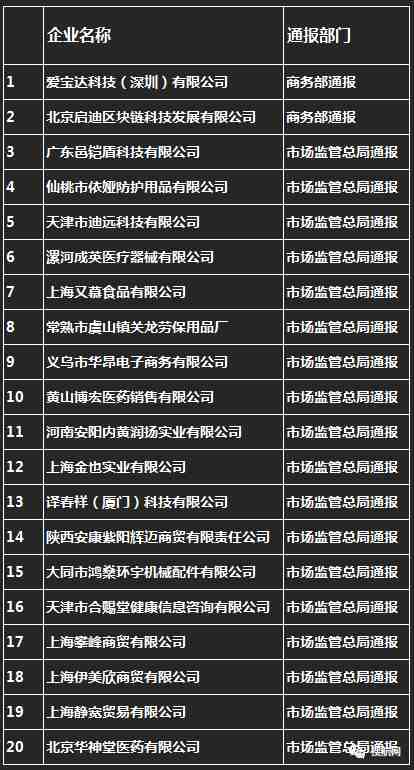
外贸出口及货代物流企业需要特别关注,确认出口企业是否进入官方的白名单,且不在市场监管总局公布的”黑名单“!
(整理:海运网、关务小二、搜航网)