“正式解封”?亚马逊FBA将恢复第三方卖家非必需品入库


据美国约翰·霍普金斯大学发布的全球新冠肺炎数据实时统计系统,截至美国东部时间4月13日晚6时,全美共报告新冠肺炎确诊57万例,死亡2.3万例,共检测293万例。
美国疫情还在不断肆虐升级,口罩仍然处于紧缺状态。而围绕美国口罩这个话题,就像“大片”一样,每隔一段时间剧情就出现神反转。
3月17日美国CDC公布了一个“优化N95呼吸器供应的策略:危机/替代策略”,批准了其它国家与N95同级别的口罩可以在美国替代使用。
名单中包含巴西、韩国、日本、澳大利亚、欧洲、墨西哥和中国(含国内的四个口罩型号:KN100、KP100、KN95、KP95),共七个国家和地区。
但在3月28日,美国食品药品管理局FDA又推出了一个新的“紧急使用管理”(Emergency-Use-Administration, 简称EUA),声明可以满足指定性能标准的可接受的呼吸器产品只有六个国家和地区。
据环球网报道,美国新闻网站BuzzFeed 3月29日的报道称,“病例激增口罩短缺,但美国拒绝中国的KN95口罩”,KN95口罩是N95口罩的中国替代品,
但美国食品药品管理局(FDA)拒绝允许其进入美国。文章质疑FDA这一决定背后有“政治原因”。
4月1日,中国外交部发言人华春莹在例行记者会上,当前疫情形势下,口罩是各国急需物资,中国国内的需求量也很大。中方企业正在开足马力、加班加点、夜以继日地生产,在满足国内需求的同时,尽量为各国防控疫情提供保障。
随着疫情的严重,美国口罩的大片剧情又有反转。
美国时间4月11日,FDA(美国食品药品监督管理局)网站上更新的文件显示,共有46家工厂位于中国的口罩生产商获得紧急使用授权(EUA)。
除3M中国、Creative Concepts等外资企业外,其余的企业都是遍布中国各地的生产商,其中包括广东、山东、河南、四川、江苏等地,在已获得紧急授权的企业中,使用中国KN95标准生产口罩的达到26家。
根据FDA文件,中国生产的口罩获得EUA授权,需要满足三个要求:
一是拥有一个或多个NIOSH(美国国家职业安全卫生研究所)认证产品的制造商,按照其他国家/地区的适用授权标准生产的其他型号的过滤式面罩呼吸器(FFR),FDA可以进行验证;
二是中国以外的其他地区授权的,FDA可以进行验证;
三是有独立的测试实验室出具的检测报告,能显示其产品性能符合适用的测试标的,FDA可以行验证。

附:获FDA紧急使用授权的厂商名单
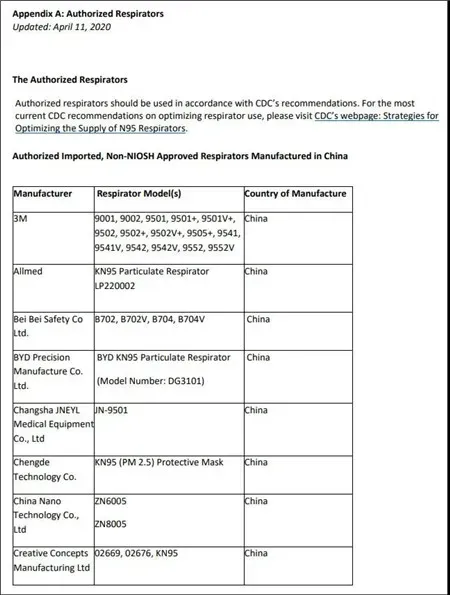
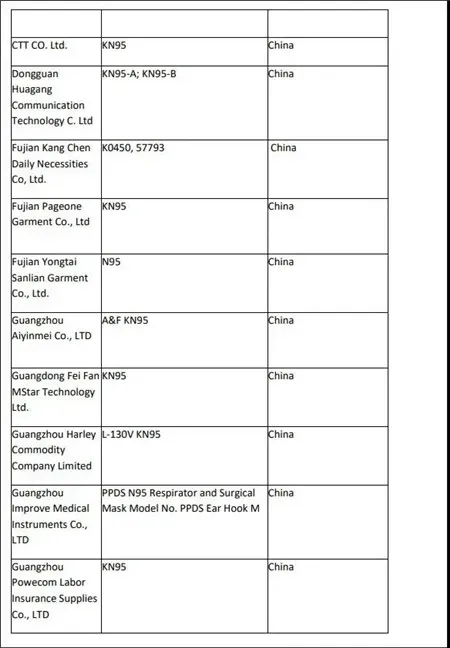
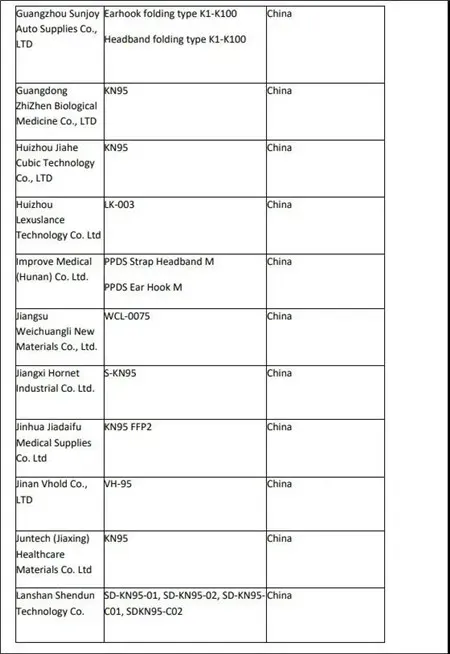
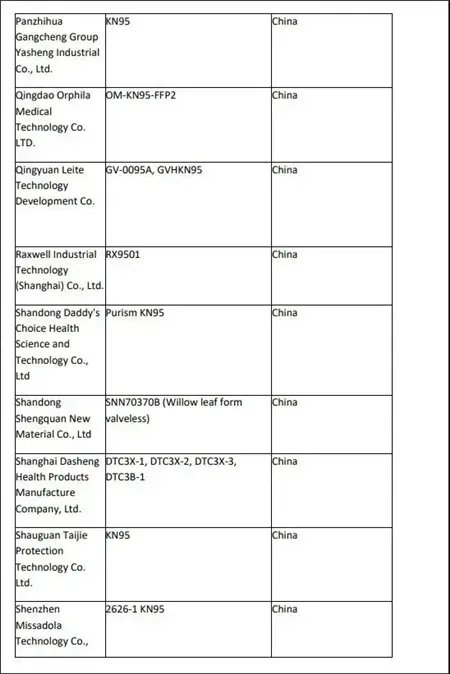
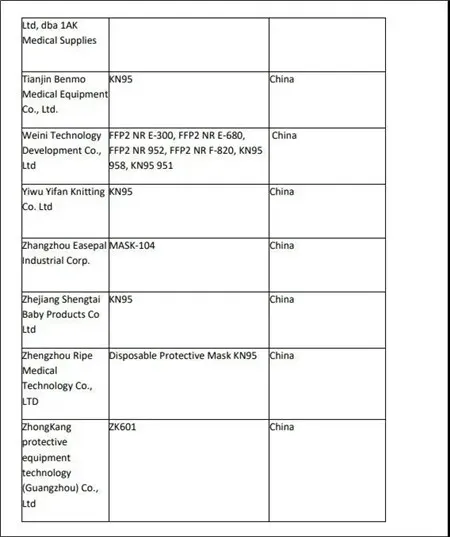
来源: SellerGrowth卖家成长

我们建了一个亚马逊卖家交流群,里面不乏很多大卖家。
现在扫码回复“ 加群 ”,拉你进群。
热门文章
*30分钟更新一次